Einführung – was der Himmel uns über Licht sagt
Sonnenlicht erscheint uns gelb am Morgen, idealerweise blau am Mittag und wechselt in einen schönen roten Sonnenuntergang. Diese beschreibt perfekt die spektrale Verteilung des Lichts, den Licht besteht aus verschiedenen Farben mit unterschiedlichen Wellenlängen. Partikel und Moleküle in der Atmosphäre streuen Licht in Abhängigkeit ihrer Größe. Große Partikel, wie Wassertropfen oder Eiskristalle, reflektieren das Licht und erscheinen weiß. Kleinere Partikel erzeugen ein Streulicht und so wird blaues Licht mit kleiner Wellenlänge mehr gestreut als rotes Licht mit längerer Wellenlänge. Das ist der Grund dafür, dass der Himmel am Mittag blau ist, aber zum Abend hin zu Rot-violett (längere Wellenlänge durch den längeren Weg des Lichts) wechselt.
Mit diesem Wissen kann das spektrale Verhalten des Lichts perfekt für die Identifizierung von Farben und Partikeln genutzt werden und das ist genau das, was optek Sensoren machen. Der Lichtstrahl einer definierten Lichtquelle geht durch eine Probe und Detektoren messen das austredende Licht, z.B. direkt bei 0° oder gestreutes Licht bei Winkeln von 11° oder 90°. Das Ergebnis ist eine Lichtintensität, die durch die Probe geht. Mittels Systemkalibrierung, unter Benutzung definierter Standards (z.B. optische Filters oder Trübungsstandards), kann dieses Ergebnis für qualitative und quantitative Analysen genutzt werden. Die Messtechnik und die gewählte Wellenlänge unterscheiden die verschiedenen Analysenmethoden.
Lambert-Beer’sches Gesetz
Eine monochromatische Lichtquelle, z.B. UV/VIS mit der Intensität I0 passiert eine verdünnte Lösung einer speziellen chemischen Substanz der Schichtdicke d und resultiert in der Intensität I. Das Licht, welches durch die Lösung geht ergibt die

welche exponentiell mit zunehmender Konzentration (c) der Lösung und mit der Schichtdicke (d) der Küvette abnimmt:
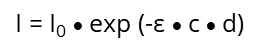
Nach Umstellen der Formel erhalten wir das “Lambert-Beer Gesetz“:
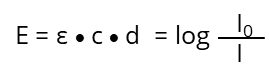
- Io: Intensität des Lichtstrahls vor der Lösung
- I : Intensität des Lichtstrahls nach dem Passieren der Lösung mit der Dicke d
- d : Schichtdicke d, oder optische Pfadlänge (cm)
- c : Konzentration der absorbierenden Substanz in mol l-1
- ε : Molarer Extinktionskoeffizient bei spezifischer Wellenlänge für diese Substanz in l mol-1 cm-1
- E : Extinktion
Im idealen Fall ist (ε), unter kontrollierten Messbedingungen (z.B. Temperatur, Lösungsmittel, pH u.s.w.) nur Abhängig von der Art der absorbierenden Substanz und der Wellenlänge (λ). Es ist eine Konstante und unabhängig von (c), aufgelistet in verschiedenen Tabellen für viele Chemikalien. Wenn die optische Pfadlänge (d) und die chemische Substanz bekannt sind (also ε), kann die unbekannte Konzentration (c) einer Substanz durch Messung der Extinktion (E) bei spezifischer Wellenlänge bestimmt werden:
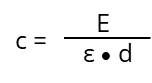
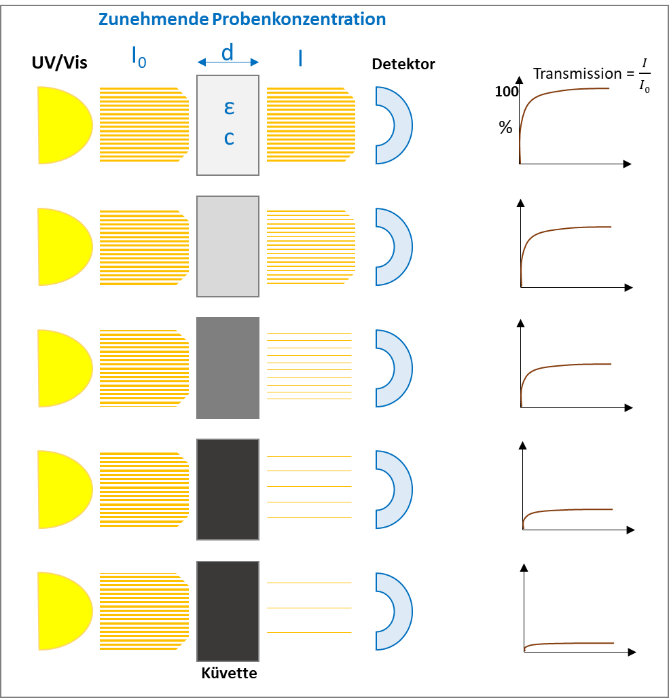
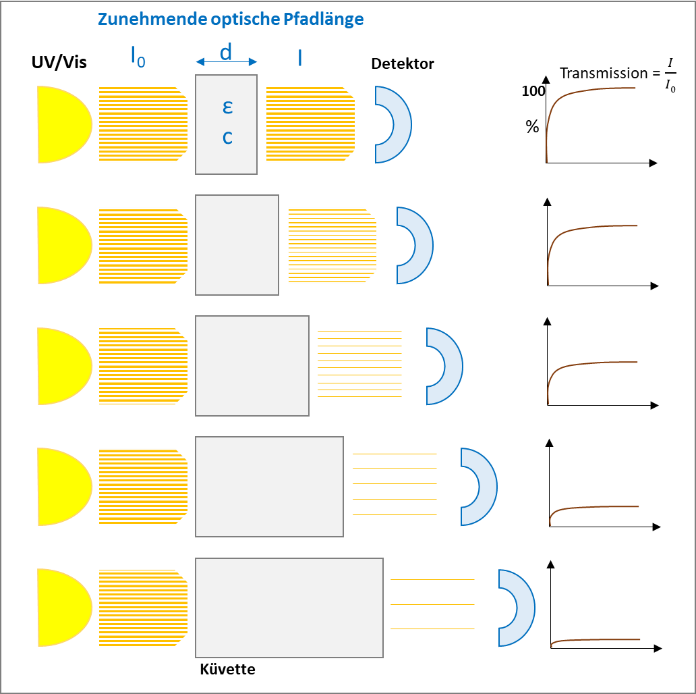
Die folgenden Abbildungen (1 und 2) visualisieren die beiden Effekte des Lambert-Beer Gesetzes:
Was wird detektiert wenn Licht durch eine Probe geht?
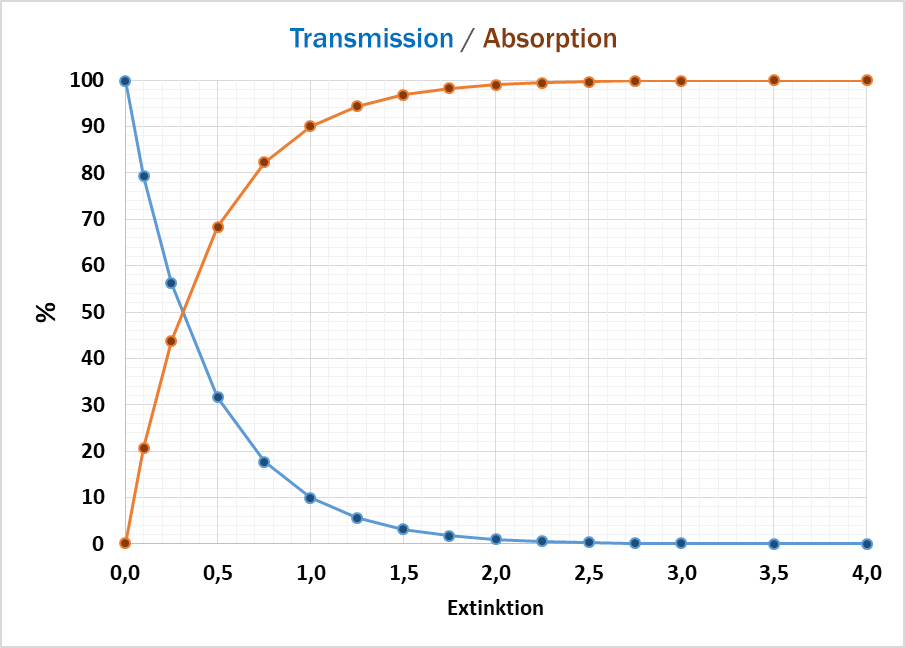
Grundsätzlich werden zwei Ergebnisse erhalten: der Wert für absorbiertes Licht oder für die Transmission.
Die Lichtabsorption, beim Durchstrahlen einer Probe, hängt hauptsächlich von der Zusammensetzung / Struktur der Probe und der Frequenz des Lichts (Wellenlänge) ab. Entsprechend dem Lambert-Beer Gesetz ist die Intensität des durchstrahlten Lichtes durch die Probe proportional zum Absorptionskoeffizienten und der optischen Pfadlänge (Schickdicke der Probe).
Absorbiert die Probe das meiste Licht, wird die Genauigkeit der Spurenanalytik von Chemikalien schlechter, weil die Absorptionskurve flacher wird und kleine Änderungen weniger zuverlässig detektiert werden können. In diesem Fall hilft eine Verdünnung der Probe oder eine kleinere optische Pfadlänge (Dicke der Probe) die Absorptionswerte zu erhöhen und viel genauere Ergebnisse zu liefern.
Auf der anderen Seite der Absorptionsskala kann zu viel Licht, das die Probe passiert, zu ungenauen Ergebnissen führen. Dann hilft eine größere optische Pfadlänge (Dicke der Probe) die Transmission zu reduzieren, wodurch der Detektor die Lichtmenge besser (genauer) verarbeiten kann.

Abbildung 4: Teilspektrum elektro-magnetischer Wellen
Die Energie einer Lichtquelle wird durch die Wellenlänge charakterisiert. Je kleiner die Wellenlänge, desto mehr Energie wird mit der elektro-magnetischen Strahlung durch eine Probe geleitet und bringt Elektronen in höhere Energiezustände oder regt Moleküle zu Schwingungen und Klappbewegungen an. Die optek Sensoren verwenden Wellenlängenbereiche des UV, VIS oder NIR in verschiedenen Konfigurationen für eine optimale Leistung bei optischen Messungen.
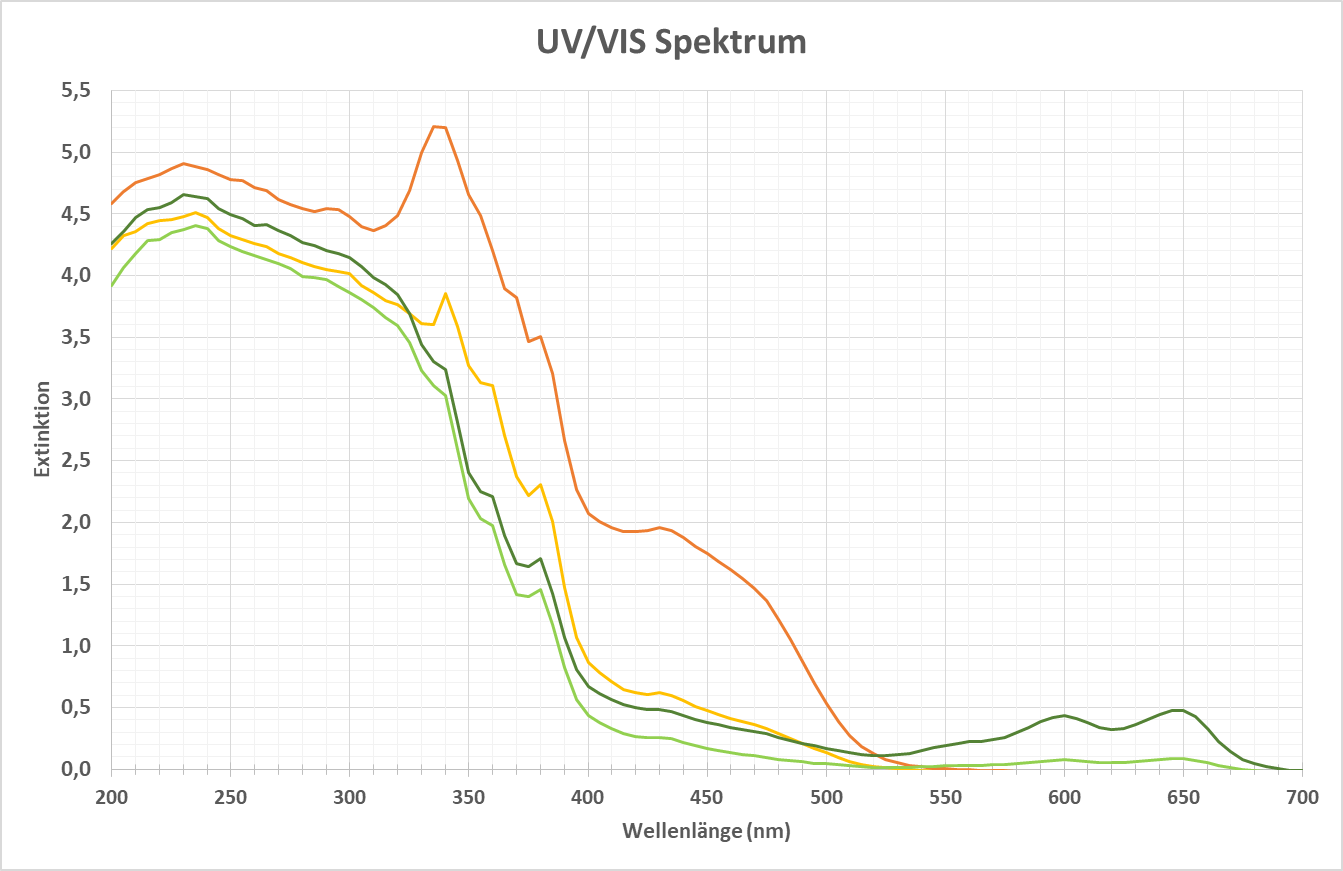
Spektrum einer Probe im UV-VIS Bereich
Wenn eine Probe mit chemischen Substanzen in den Strahl einer Lichtquelle der Energie z.B. von 200 bis 700 nm Wellenlänge gebracht wird, absorbieren die Moleküle Licht bei bestimmten Wellenlängen. Das oben gezeigte Spektrum kann das Ergebnis der Messungen sein. Es hängt von der Charakteristik der chemischen Substanz ab, den Wellenlängenbereich so zu wählen, dass Peaklage und Höhe dazu geeignet sind, z.B. Farbe, Konzentration, Strukturänderungen (z.B. durch pH-Änderungen) oder Trübungen zu bestimmen. Die Detektion des durch die Probe gehenden Lichtes kann in verschiedenen Richtungen erfolgen. Die übliche Technik ist die Messung der Transmission (oder reziproke Absorption) bei einem Detektionswinkel von 0°.
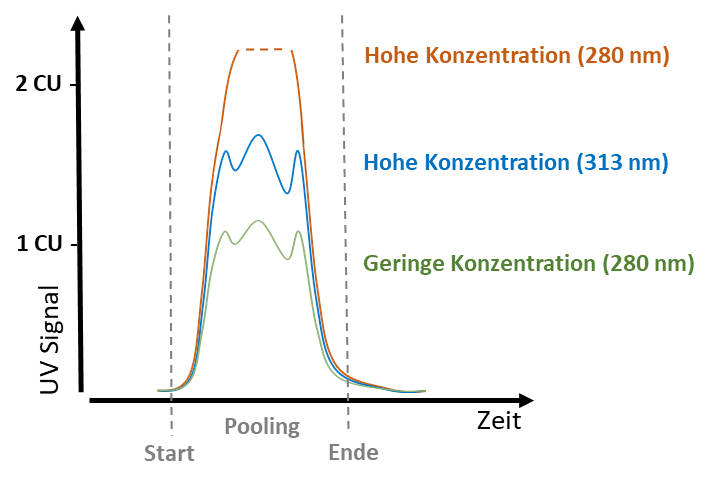
In der Biotechnologie wird zur Charakterisierung des Poolingstatus von Proteinen oft die Wellenlänge von 280 nm für geringe Konzentrationen verwendet. Dieser Peak bei 280 nm überschreitet aber bei höheren Konzentrationen schnell den maximalen Messbereich und verliert zudem die Peakstrukturen. Deshalb werden höhere Konzentrationen an der Peakflanke bei > 300 nm gemessen, wo auch wieder Peakstrukturen zur Identifizierung aufgelöst werden können.